Плътност на водата (H₂O)
Какво е плътност?
Плътност е скаларна физическа величина, дефинирана като отношение на масата на тялото към заемания от него обем, или като производна на масата спрямо обема.
Формула за плътност
ρ = M / V
Където
- ρ (ро) е плътността - кг/м³
- M е масата на тялото в кг
- V е заеманият от тялото обем в м³
 |
| Плътност на водата |
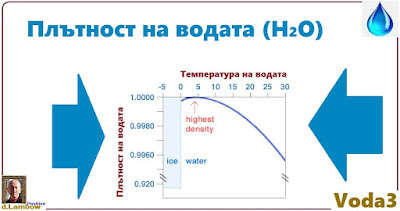
Плътност на водата
За разлика от почти всички други вещества, чиято плътност се увеличава през цялото време, докато се охлаждат, водата има най-висока плътност При – + 4oC - 1 g/cm3
- - Плътност на водата - (При – 4 °C) - 1000 кг/м³
- - Плътност на водната пара - (При – 100 °C) - 0,598 кг/м³
Значение на плътността на водата
Плътността на водата не е константа, нейната стойност зависи, При – условие на постоянно налягане, от два фактора:
- - температура и
- - соленост (количеството на разтворените в нея соли).
Така например, плътността на чистата прясна вода При – температура 20 ° C и налягане от 1 атм е 998,23 kg / m3, а плътността на морската вода на повърхността на океана е приблизително 1027 kg / m3.
Плътността на водата като функция от температурата
По-долу е показана промяната в плътността на чистата вода в зависимост от температурата:
Плътността на водата като функция от температурата
По-долу е показана промяната в плътността на чистата вода в зависимост от температурата:
- - При – 30 °C — 0,9839 g/cm³;
- - При – 20 °C — 0,9935 g/cm³;
- - При – 10 °C — 0,9982 g/cm³;
- - При – 0 °C — 0,99987 g/cm³;
- - При – 1 °C — 0,99993 g/cm³;
- - При – 2 °C — 0,99997 g/cm³;
- - При – 3 °C — 0,99999 g/cm³;
- - При – 4 °C — 1.00000 g/cm³;
- - При – 5 °C — 0,99999 g/cm³;
- - При – 6 °C — 0,99997 g/cm³;
- - При – 7 °C — 0,99993 g/cm³;
- - При – 8 °C — 0,99988 g/cm³;
- - При – 9 °C — 0,99981 g/cm³;
- - При – 10 °C — 0,99973 g/cm³;
- - При – 15 °C — 0,99913 g/cm³;
- - При – 20 °C — 0,99823 g/cm³;
- - При – 25 °C — 0,99707 g/cm³;
- - При – 30 °C — 0,99562 g/cm³;
- - При – 40 °C — 0,99224 g/cm³;
- - При – 50 °C — 0,98807 g/cm³;
- - При – 60 °C — 0,98324 g/cm³;
- - При – 70 °C — 0,97781 g/cm³;
- - При – 80 °C — 0,97183 g/cm³;
- - При – 90 °C — 0,96534 g/cm³;
- - При – 100 °C — 0,95838 g/cm³.
|
|
Аномална плътност на водата
Както виждаме, плътността на водата в течно състояние, отначало, когато температурата се повиши до 4 градуса по Целзий, се увеличава и след това намалява от 4 °C и нагоре. Тоест при 4 ° C плътността достига максималната си стойност. Следните факти и явления са свързани с аномалията на плътността на водата:
- - При замръзване водата се разширява;
- - Плътността на водата в твърдо състояние - ледът е по-ниска от PV в течно състояние;
- - Водата има нисък коефициент на разширяване и свиване.
Отлична илюстрация на аномалията с плътността на водата е например ледът. Той не потъва, защото плътността му е по-малка от тази на водата.
Значение за планетата
Свойството на водата, поради което максималната й плътност се достига при +4 °C, е от голямо значение за цялата ни планета. Например, поради това особено свойство, езерата и другите водни басейни замръзват отгоре, което позволява на всички форми на живот в тях да оцелеят по време на тежки студове, под леда.
Уникалните свойства на плътността на водата още веднъж потвърждават, че в природата всичко е в хармонична връзка, която не може да бъде нарушавана по никакъв начин, без да плащаме последици за това.
----------------









